Aquelas que afectan o sistema nervioso e ós músculos. As enfermidades máis frecuentes e coñecidas pola población son:
A demencia non é unha enfermidade específica, senón que se trata dun termo descritivo para un conxunto de síntomas que á súa vez pode ser causado por diferentes enfermidades que afectan ó cerebro. As persoas con demencia teñen alteradas as súas capacidades intelectuais de forma significativa, de tal maneira que lles interfire na súa actividade normal e nas relacións sociais. Asimesmo, perden a capacidade para resolver problemas e manter o control sobre as súas emocións. Con frecuencia poden experimentar cambios de personalidade e ter problemas de comportamento, como axitación, delirios e alucinacións.
Aínda que a perda de memoria é un síntoma moi común de demencia, perder memoria en si non significa que unha persoa teña demencia. Incluso algúns enfermos non teñen afectada de forma significativa a súa memoria ó comezo do proceso. Os neurólogos soamente diagnostican demencia se dúas ou máis funcións cognitivas cerebrais (memoria, linguaxe, xuízo, orientación) están afectadas de forma relevante nunha persoa con plena consciencia.
As formas ou causas de demencia son múltiples. Aínda que a xente identifica demencia con enfermidade de Alzheimer, esta é unicamente a forma máis común, supoñendo un 60-70% dos casos. Outras formas tamén frecuentes son a demencia vascular (por exemplo: tras ter sufrido un ictus), a demencia por corpos de Lewy e un complexo grupo de enfermidades que orixinan a demencia frontotemporal (dexeneración do lóbulo frontal do cerebro con alteracións precoces na personalidade e no comportamento do individuo). En ocasións os límites entre estas diferentes formas de demencia son difusos, sobre todo ó inicio ou cando coexisten varias á vez, o que se denomina demencia mixta.
Os neurólogos ademais temos que identificar condicións que poidan causar demencias reversibles, tratables ou incluso pseudodemencias, como son os efectos adversos de medicacións, alteracións metabólicas e endócrinas, déficits nutricionais, infeccións, intoxicacións, tumores cerebrais, anoxia e hipoxia cerebral (falta de osíxeno ó cerebro), enfermidades do corazón e dos pulmóns.
A pesares de ser moi común en persoas maiores, nunca debemos pensar que forma parte do envellecemento normal,e aínda que ás veces custa diferenciar as fallas propias da idade do comezo dunha demencia, o neurólogo ten ferramentas para elo.
A demencia é unha das principais causas de discapacidade e dependencia entre as persoas maiores de todo o mundo, supoñendo en moitas ocasións un tremendo sufrimento para o paciente pero tamén para os seus coidadores e familiares.
EPIDEMIOLOXÍA: AS CIFRAS
En España hai ó redor de 600.000 persoas con demencia e cerca de 400.000 con enfermidade de Alzheimer. A prevalencia é catro veces maior en grupos de maior idade, en mulleres e en rexións do centro e noroeste de España. Calcúlase que en Galicia hai uns 63.000 afectados, pero a falta de rexistros fai pensar que esta cifra pode ser maior ó haber casos sen diagnosticar.
Galicia é unha comunidade envellecida na que se espera un crecemento exponencial na carga de trastornos neurodexenerativos crónicos como a demencia.
¿CÓMO SE DIAGNOSTICAN?
Na maior parte das demencias non hai un test ou unha proba que as diagnostique con seguridade. O diagnóstico débese facer por médicos expertos e asenta en tres pilares fundamentais, que son por orde de importancia:
- Os síntomas que refire o paciente e a súa familia
- A exploración do enfermo, sobre todo a neuropsicolóxica (test con preguntas que exploran as diferentes capacidades cognitivas)
- Realizaranse estudios sempre encamiñados a descartar outras enfermidades, pero tamén existe xa a posibilidade de facer probas que indirectamente nos orientan á causa da demencia que padece o enfermo
Un diagnóstico precoz e correcto:
- Beneficia ó coidador: reduce o síndrome do coidador queimado, a depresión e outros índices de saúde mental, mellora a interpretación e o manexo dos trastornos de conduta.
- E beneficia ó enfermo: permite a instauración precoz dun tratamento específico, reduce a necesidade de medicación para os trastornos de conduta e mellora as actividades da vida cotiá.
TRATAMENTO
- Farmacolóxico: a día de hoxe dispoñemos de medicamentos específicos para o Alzheimer e algunha outra demencia progresiva. Aínda que estes fármacos non frean a enfermidade nin reverten o dano cerebral, poden mellorar certos síntomas e enlentecer a progresión. Isto á súa vez mellora a calidade de vida do individuo, alivia a sobrecarga do coidador e atrasa a institucionalización de estes enfermos (ingreso en centros de día ou residencias). Investígase ademais se estes fármacos poden ser útiles en outras demencias.
- Non farmacolóxico: moitas persoas afectadas, sobre todo en estadios precoces, poden beneficiarse de terapias de estimulación cognitiva nas que se potencian as funcións máis comprometidas e se desenvolven estratexias de compensación utilizando os recursos cognitivos que aínda están preservados. De esta maneira mantense un maior grao de autonomía e funcionalidade. Son recomendables tamén a terapia ocupacional e o exercicio físico.
¿Qué é un ictus?
A palabra ictus procede do latín e significa golpe ou ataque. Fai referencia a calquera trastorno da circulación cerebral, xeralmente de comezo brusco, que pode ser consecuencia da interrupción do fluxo sanguíneo a unha parte do cerebro (isquemia) ou a rotura dunha arteria ou vea cerebral (hemorraxia).
Popularmente empréganse múltiples nomes para denominalo: infarto cerebral, trombosis, embolia, derrame cerebral, apoplexía… o que condiciona confusión en canto ó concepto e á diferenciación entre os diferentes tipos.
O ictus é a primeira causa de mortalidade entre as mulleres españolas e a segunda nos varóns, según datos do Grupo de Estudio de Enfermidades Cerebrovasculares da Sociedade Española de Neuroloxía. En Europa falecen 650.000 persoas anualmente por esta causa e, deles, 40.000 son españois. Ó ano detéctanse uns 120.000-130.000 casos novos. De feito, cada seis minutos ten lugar un ictus en España.
En España, o ictus provoca máis mortalidade e discapacidade que os accidentes e o Alzheimer xuntos.
¿Cáles son los tipos de ictus?
a) Isquémicos:
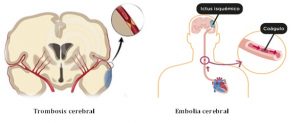
1. Ictus trombótico, aterotrombótico ou trombose cerebral: é aquel no que o material que impide o paso de sangue (trombo) nun vaso formouse no propio vaso.
2. Ictus embólico ou embolia cerebral: é aquel no que trombo está orixinado por un coágulo de sangue que se formou lonxe do lugar da obstrucción, normalmente no corazón.
3. Ictus hemodinámico: o déficit de aporte sanguíneo débese a un descenso na presión sanguínea, por exemplo, cando se produce unha parada cardíaca ou unha arritmia grave, pero tamén pode ser debido a unha situación de hipotensión arterial grave e mantida.
4. Ataque isquémico transitorio: é un tipo de ictus no que o doente padece transitoriamente tódolos síntomas cos que cursa un ictus (con frecuencia só dura uns minutos), pero éstes desaparecen sen deixar ningunha secuela. Tamén é unha emerxencia médica.
b) Hemorráxicos:
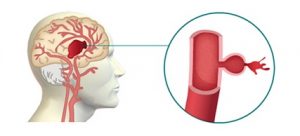
1. Hemorraxia intracerebral: prodúcese cando unha arteria cerebral profunda rompe e deixa sair o seu contido sanguíneo, o cal se esparce entre o tecido cerebral circundante, presiónandoo e danándoo.
2. Hemorraxia subaracnoidea: é unha hemorraxia localizada entre a superficie do cerebro e a parte interna do cráneo. A súa causa máis frecuente é a rotura dun aneurisma arterial (anomalía na parede dunha arteria).
¿Qué síntomas podo ter?
Os síntomas do ictus son moi variados e dependen da área do cerebro que se vexa afectada. A clave para identificar que os síntomas son debidos a un ictus é o seu inicio brusco.
Entre os principales síntomas que debemos ter en conta son:
1. Forza: perda de forza que pode afectar a brazos ou pernas, ou á cara (tórcese a boca)
2. Fala: non pronunciar ben, ou o que dicimos é incoherente, confundimos ou cambiamos palabras…
3. Sensibilidade: formigueo ou acartonamento que pode afectar a cara, brazo e/ou perna.
4. Outros: perda de visión brusca nun ollo, visión doble, inestabilidade ó camiñar, dor de cabeza
moi intensa (“a dor máis intensa da miña vida”), etc.
A identificación inmediata dos síntomas do ictus é crucial para salvar a vida e para conseguir as menores secuelas posibles. Está demostrado que los doentes tratados dende o primeiro momento por neurólogos logran unha recuperación casi total ou con moi poucas secuelas.

¿Qué facer e qué non facer en caso de síntomas suxestivos de ictus?
a) Qué facer:
1. Avisar a un familiar que me acompañe.
2. Avisar de inmediato ó 061 ou acudir directamente ó hospital de referencia se se vai retrasar a ambulancia.
3. Anotar la hora de inicio dos síntomas.
b) Qué non facer:
1. Esperar a que se me pase.
2. Tomar Aspirina.
3. Non avisar a ninguén por no molestar.
4. Avisar ó médico de cabeceira para que me veña ver á casa cando poida
NON HAI QUE ESQUECER QUE É UNHA URXENCIA MÉDICA
¿Qué tratamientos existen para el ictus?
Unha das claves no control do ictus é a atención inmediata e especializada por un Neurólogo.
O código ictus é un protocolo de actuación prehospitalario ou extrahospitalario baseado no recoñecemento precoz dos signos e síntomas dun ictus, coa consecuente priorización de coidados e o traslado inmediato a un Centro Capacitado daqueles doentes candidatos a beneficiarse dunha terapia de reperfusión e de coidados especiais nunha Unidade de Ictus. Os obxectivos do Código
Ictus son os seguintes:
- Disminuir o tempo entre o inicio do ictus e o acceso a un diagnóstico e tratamento rápido.
- Incrementar o número de doentes con ictus tratados con fibrinolise.
- Reducir a dependencia dos doentes para realizar as actividades da vida diaria, a necesidade de coidados permanentes e incluso reducir a mortalidade.
Canto menos tempo se tarde en chegar a un diagnóstico, máis cedo se podería administrar un tratamento axeitado co que se reduciría a cantidade de tecido cerebral con danos irreversibles: TEMPO É CEREBRO.
Dependendo do tipo de ictus e do tempo de evolución dos síntomas, pódense aplicar diferentes tratamentos:
a) No caso de los ictus isquémicos:
1. Axentes trombolíticos (fibrinolisise): para intentar destruir os coágulos que están producindo o infarto cerebral e recanalizar o vaso sanguíneo obstruido. Estes fármacos só se poden empregar nas primeiras horas do ictus por motivos de seguridade e nunhas condicións moi concretas.
2. Trombectomía mecánica: en casos moi seleccionados, se non é posible administrar a fibrinolise ou ésta non é eficaz, inténtase a extracción do coágulo empregando un dispositivo que é introducido a través dunha arteria para intentar chegar ó trombo e retiralo.
3. Antiagregantes plaquetarios e anticoagulantes: son fármacos que se administran na maioría dos ictus isquémicos para previr que se repita. En función da causa do ictus e das características do doente determínase cal é o máis axeitado para cada persoa.
b) No caso das hemorraxias:
1. Se se producen por alteracións na coagulación do sangue baséase o tratamento en intentar reverter o problema se é posible.
2. Se son producidas por malformacións nos vasos (por exemplo, un aneurisma) tentarase “desconectalas” da circulación mediante cirurxía ou técnicas endovasculares, para evitar que poidan romper de novo e sangrar.
¿Cómo se pode previr?
Aínda que contamos con medidas terapéuticas para intentar reducir ó mínimo a lesión cerebral producida por un ictus, un dos mellores tratamentos que existen para as enfermidades cerebrovasculares é a súa adecuada prevención, e ésta comeza pola modificación dos principais factores de risco «tratables».
O ictus é máis frecuente a partir dos 55 anos e o seu risco aumenta coa idade. Estímase que máis do 21% da poboación maior de 60 anos do noso país, case dous millóns de personas, presenta un alto risco de sufrir un ictus nos próximos 10 anos.
Pero ademáis da idade, existen outras causas de risco como son: a hipertensión arterial, as arritmias cardiacas ou outras enfermidades do corazón, a diabetes mellitus, o colesterol alto, a obesidade, o sedentarismo, fumar e o consumo excesivo de alcol, entre outros.
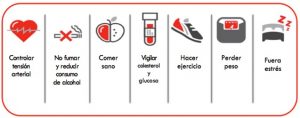
Recomendacións saudables:
1. EXERCICIO: Camiñe e faga exercicio con regularidade: polo menos 3 días á semana durante polo menos 30 minutos. O exercicio máis sinxelo , ecolóxico e con menos riscos é camiñar.
2. DIETA EQUILIBRADA:
- Consumo de frutas, verduras e peixe.
- Alcohol: beba alcol con moderación, non máis de 2 vasos pequenos de viño ó día.
- Colesterol: controle o su colesterol cunha dieta equilibrada, baixa en graxas e, cómo non, con exercicio!
- Peso: A obesidade asociase a maior risco de ictus debido, entre outras cousas, a que a obesidade se asocia a hipertensión arterial, diabetes e cifras máis elevadas de colesterol
3. TENSION ARTERIAL: para elo debe controlar o peso, reducir a inxesta de sal nas comidas e… facer exercicio!
4. GLUCOSA: controle as súas cifras de azucre no sangue
5. CORAZÓN: coide o seu corazón, xa que as enfermidades do corazón son unha causa importante de ictus.
6. FUMAR: Nada!
7. FORA ESTRÉS
Despois do ictus
1. Siga as recomendaciós do seu Neurólogo.
2. Manteña hábitos de vida saudables: tentar modificar os factores de risco “tratables”, expostos previamente, é tan importante como a toma da medicación.
3. Rehabilitación: a rehabilitación busca minimizar os déficits ou discapacidades experimentadas polo doente que sufriu un ictus. Trátase dun proceso activo que require a colaboración e capacidade de aprendizaxe do doente e da súa familia. Non so é importante a rehabilitación física, se non tamén o apoio psicolóxico por parte da familia e, se fora preciso, tamén dun profesional.
A lesión neurolóxica pode recuperarse por completo, recuperarse só en parte ou non chegar a recuperase nunca: esto vai depender da gravidade do ictus e da rehabilitación. Por tanto é importante lembrar que nos sempre é posible acadar unha recuperación completa, e que o principal obxectivo é axudar ó doente a adaptarse.
¿Cómo evoluciona a recuperación?
A melloría clínica soe ser máis evidente no primeiro mes e tende a manterse ata o terceiro mes. Entre o terceiro e sexto mes tal melloría é menor, e con cambios progresivamente menores ata pasado un ano. En xeral, establécese que a partir do sexto mes é cando ten lugar a estabilización, pero hai que ter en conta que as alteracións da linguaxe e do equilibrio poderían seguir mellorando
ata pasados 2 anos.
De forma global estímase que entre os sobreviventes do ictus o 44% quedan cunha dependencia funcional.
Débese manter unha vida o máis activa posible, dentro das limitacións que existan.
A neuroloxía é a especialidade médica que se encarga de coidar ós enfermos con epilepsia.
A epilepsia é a principal enfermidade neurolóxica crónica, xa que afecta ó 0.8% da poboación en Galicia, o que supón aproximadamente 18.000 persoas. No mundo estímase que 50 millóns de persoas padecen epilepsia.
Cando a maioría das persoas escoitan a palabra “epilepsia” na súa mente aparece a escena dunha persoa que cae ó chan inconsciente, ten sacudidas incontrolables, babea e perde o control da vexiga. Sen embargo, este tipo de crises, que é a convulsiva xeneralizada, é solo un tipo de epilepsia. Hai moitos outros tipos de epilepsia, cada un acompañado dun conxunto diferente de síntomas.
A epilepsia é un trastorno do cerebro no cal as súas células, que se chaman neuronas, transmiten a veces os sinais de forma anormal. As neuronas envían sinais a outras neuronas e ós músculos para producir pensamentos, sentimentos e accións. A epilepsia altera a actividade normal das neuronas e pode causar sensacións, emocións e comportamentos estraños, espasmos musculares e perda de coñecemento.
A epilepsia pode afectar a calquera persoa, independentemente do sexo, idade ou raza. De feito algunhas persoas célebres padeceron epilepsia na historia, como Xulio César, NapoleóN Bonaparte ou Agatha Cristie, Isaac Newton e Beethoven.
Os nenos e as persoas maiores son os que teñen máis risco de desenvolver a enfermidade. De feito calcúlase que 15 de cada 1.000 persoas maiores de 75 anos sofren epilepsia.
A falta de coñecementos sobre a enfermidade ocasiona que moitos pacientes sufran discriminación e estigma social. Por exemplo, en países desenvolvidos como o noso, Alemaña, Italia ou Estados Unidos unicamente están empregados a metade dos pacientes con epilepsia en idade laboral, a miúdo en traballos por debido da súa capacidade potencial.
Na actualidade dispoñemos de numerosos fármacos antiepilépticos que conseguen controlar a enfermidade con un adecuado seguimento por parte dos neurólogos en ata un 85% dos casos. Aínda que en ocasións precísanse varios fármacos para poder levar unha calidade de vida plena.
Nos pacientes que non se controlan con tratamento médico, en ocasións é posible realizar unha intervención cirúrxica ou colocar un implante no nervio vago, similar a un marcapasos cerebral, para que desta maneira poidan estar controlados.
Se padeces epilepsia, ou crees que puideras sufrila, debes ir ó Neurólogo, xa que somos os únicos expertos na túa enfermidade.
Os neurólogos estamos comprometidos co obxectivo de mellorar a calidade de vida dos nosos doentes.
O termo trastornos do movemento engloba un grupo de enfermidades nas cales predominan as alteracións na forma e na velocidade dos movementos corporales. A maioría destes trastornos están asociados coa disfunción dunha estructura cerebral chamada ganglios basales.
Poden clasificarse en dous grandes grupos:
1.- Trastornos do movemento hipocinéticos: caracterizados por lentitude do movemento (bradicinesia) e diminución do movemento espontáneo (hipocinesia), ademáis de rixidez (exceso de tono muscular por falta de relaxación).
Neste grupo englóbanse:
1.1.- Síndromes parkinsonianos: caracterizados por acinesia e rixidez, bradicinesia (movementos lentos e de pouca amplitude), con ou sen tremor. A enfermidade de Parkinson é a causa máis frecuente e importante do parkinsonismo, se ben hai outras causas que deben de ter en conta no diagnóstico diferencial.
As enfermidades mais frecuentes que xeneran estes síndromes son:
1.1.1.- Enfermidade de Parkinson: é a causa máis frecuente de parkinsonismo. Prevalencia entre 100 e 200 casos por cada 100.000 habitantes. A súa frecuencia aumenta coa idade, sobre todo a partires dos 60 anos. É máis frecuente en varóns. Caracterízase pola presencia de: tremor de repouso, bradicinesia, rixidez e inestabilidade postural, podendo presentar outros síntomas, como o estreñimento ou a hiposmia. O diagnóstico é clínico, apoiado nalgúns casos de determinadas probas complementarias. A día de hoxe non dispoñemos de cura pero sí de tratamento para moitos dos síntomas que produce.
1.1.2.- Outras enfermidades que cursan con parkinsonismo son:
- Atrofia múltiple de sistemas
- Parálise supranuclear progresiva
- Enfermidade por corpos de Lewy
- Dexeneración córticobasal
- Demencia frontotemporal
- Parkinsonismo secundario a fármacos e a toxinas
- Parkinsonismo vascular
- Parkinsonismo postinfeccioso
1.2.- Síndrome da persona ríxida: englóbase dentro dos cadros clínicos de actividade muscular contínua. Trátase dunha enfermidade por anticorpos que actúan contra a enzima sintetizadora do ácido gamma-aminobutírico.
1.3.- Síndrome neuroléptico maligno: trátase dunha reacción idiosincrática a determinados fármacos (bloqueadores dos receptores de dopamina) que produce un cadro de inicio agudo con rixidez intensa, febre, taquicardia, sudoración e deterioro do nivel de consciencia.
2. – Trastornos do movemento hipercinéticos: caracterizados por un exceso de movemento ou por movementos anormales involuntarios (discinesias). Inclúen ás seguintes entidades: tremor, distonía, corea, balismo, atetose, tics, mioclonías, hiperekplexia (ou enfermidade do sobresalto), espasmo hemifacial, esterotipias, acatisia e outros trastornos do movemento. Moitas veces o diagnóstico diferencial destas entidades é complexo porque se solapan unhas con outras.
Os trastornos mais comunes englobados nesta categoría son:
2.1.- Tremor: movemento oscilatorio rítmico dunha parte do corpo debido a contraccións rítmicas de músculos agonistas e antagonistas (uns cunha determinada función e outros coa contraria). Dentro deste grupo o máis frecuente é o tremor esencial. Outras causas de tremor son o tremor fisiolóxico esaxerado, tremor mentoniano, tremor relacionado con fármacos, con alteracións metabólicas (hipertiroidismo), tremor ortostático, tremor cerebeloso, tremor neuropático (entre outros).
2.2.- Distonía: neste trastorno neurolóxico aparece unha actividade muscular mantida que produce movementos de torsión repetitivos e posturas anormales. Prodúcese pola contracción simultánea de músculos agonistas e antagonistas.
2.3.- Corea: consiste en movementos irregulares, impredecibles, abruptos e breves que cambian dunha zona corporal a outra de forma aleatoria. Dentro deste grupo atópanse a corea de Huntington e a de Sydenham entre outras. Outras formas de corea son a coreoatetose (movementos serpenteantes) e o balismo (grao grave de corea con movementos bruscos e de gran amplitude)
2.4.- Tics: son movementos bruscos, breves e repetitivos, estereotipados, que varían en intensidade e aparecen de forma irregular. Pódense suprimir voluntariamente por un período variado de tempo, pero esta supresión habitualmente séguese dun período rebote no que aumenta o número de tics. Unha entidade que presenta estos movementos é o síndrome de Tourette.
2.5.- Mioclonías: son movementos bruscos, rápidos e moi breves, de amplitude variable, producidos ben por contraccións musculares (mioclonías positivas) ou por perda brusca do tono muscular (mioclonías negativas e asterixe). As mioclonías poden ter múltiples causas, dende alteracións metabólicas ata lesións cerebrales e medulares.
2.6.- Síndrome de pernas inquedas: caracterízase pola aparición de molestias nas pernas (formigueos, sensación de intranquilidade, dolor…) que aparecen en situación de repouso, habitualmente vespertinas-nocturnas, que obrigan a mover as pernas para conseguir alivio.
2.7.- Outras: Hiperekplexia. Acatisia. Estereotipias.
3- Dentro dos trastornos do movemento existe un terceiro grupo, englobado baixo o nome de ataxias. A ataxia non é unha enfermidade, se non que é un síntoma que pode ser debida a alteracións en diversas partes do sistema nervioso, máis habitualmente no cerebelo. Denomínase ataxia á falta de coordinación, que se pode manifestar como unha falta de equilibrio ó andar (ataxia da marcha) ou unha falta de coordinación nos movementos das mans, que se manifesta con dificultade para alcanzar un obxectivo concreto (dismetría).
A ataxia pode deberse a alteracións en varios dos sistemas que controlan o equilibrio e a coordinación, como son o cerebelo, as aferencias sensitivas ou o laberinto e o sistema vestibular.
Así as ataxias divídense en:
3.1.- Ataxia cerebelosa: por alteración no cerebelo ou nas súas conexións. Cursa con alteración da marcha na cal se aumenta a base de sustentación, con pasos irregulares; incoordinación de movementos e alteración da fala (fala tremorosa, con arrastre das palabras, chamada disartria).
3.2.- Ataxia sensorial: por unha afectación nas vías sensitivas que informan sobre a posición das articulacións. Pode afectarse por un problema nos nervios periféricos, por problema na parte posterior da médula espinal ou ben por alteración das conexións entre o cerebelo e a médula. Habitualmente cursa con trastorno do equilibrio que empeora ó pechar os ollos.
3.3.- Ataxia laberíntica: por afectación do oído interno. Hai alteración da marcha pero non hai alteración da fala nin da coordinación das extremidades.
Dor de cabeza: ¿É frecuente?
No noso medio, a dor de cabeza, tamén coñecida como cefalea, constitúe o primeiro motivo de consulta dos doentes que requiren asistencia neurolóxica nas consultas de Neuroloxía.
Nun estudo español a máis de dous mil entrevistados, un 74% referiu padecer ou ter padecido dores de cabeza ó longo da súa vida. Esta proporción varía entre o 69% dos varóns e o 79% das mulleres, o que reflexa a influencia do sexo na súa aparición. Outros estudos elevan a cifra, indicando que ata un 95% das persoas terán dor de cabeza nalgún momento da súa vida.
¿Existen distintos tipos de dor de cabeza?
Si. Enténdense por cefaleas primarias as que non son atribuíbles a outro trastorno, mentres que as cefaleas secundarias son unha manifestación doutra enfermidade ou proceso capaz provocar dor de cabeza, como poden ser o consumo de alcol, un proceso febril ou padecementos no nariz ou senos paranasais, entre outros.
As cefaleas primarias máis frecuentes son: a tensional (60% do total de dores de cabeza) e a migraña (tamén coñecida como xaqueca) con ou sen aura (15%). Moito máis raras dentro das cefaleas primarias son as chamadas trixémino-autonómicas, entre as que a principal é a cefalea en racimos ou de Horton, que supón o 0,2-0,3% do total de dores de cabeza.
¿Pode a migraña ser un proceso crónico?
Si. Entre un 2 e un 3% de doentes con migraña evoluciona a unha situación coñecida como migraña crónica, caracterizada por cefalea durante polo menos 15 días ó mes, dos que ó menos 8 días ó mes son de dor con características de migraña.
Dóeme a cabeza: ¿preciso unha proba de imaxe?
Probablemente non. Para a maioría dos doentes con cefalea son suficientes a historia clínica e a exploración neurolóxica para chegar a un diagnóstico. So en determinados casos se precisarán unha ou máis probas complementarias, como poden ser a tomografía computerizada (tamén coñecida como TAC ou escáner) ou a resonancia magnética cerebral. O uso rutineiro destas probas de imaxe non está aconsellado nas cefaleas primarias máis frecuentes (cefalea tensional e migraña).
¿É certo que a dolor de cabeza pode verse agravada polos calmantes?
Si. A cefalea por abuso de analxesia é unha entidade ben coñecida e frecuente: afecta ó 1-2% da poboación xeral e predomina en mulleres. Consiste no empeoramento ou cronificación dunha cefalea primaria debido ó uso excesivo de medicación sintomática empregada para o alivio da dor inmediata, como son os analxésicos simples (antiinflamatorios non esteroideos, paracetamol, aspirina), opiáceos, fármacos específicos para a migraña (ergóticos ou triptanes) ou unha combinación deles. Considérase coma un uso excesivo a toma dos analxésicos simples en máis de 15 días ó mes, ou dos outros fármacos en máis de 10 días ó mes.
É importante tratar de previr esta situación, dado que revertila pode ser difícil.
O tratamento da cefalea por abuso de medicación basease na retirada do fármaco responsable, e non é infrecuente que nos días seguintes se agrave a dor de cabeza e aparezan náuseas, vómitos, ansiedade e insomnio.
Texto adaptado da Guía Oficial de Práctica Clínica en Cefaleas da Sociedade Española de Neuroloxía (2015).
A esclerose múltiple (EM) é unha enfermidade crónica do sistema nervioso central (SNC), potencialmente invalidante e para a que na actualidade non se dispón de tratamento curativo. No mundo padécena uns 2,8 millóns de persoas, en Europa preto de 1.300.000 e en España preto de 50.000. Galicia é a área coa prevalencia máis alta de España, cunha incidencia anual algo superior a 8 doentes por cada 100.000 habitantes, o que supón que ten que haber uns 4.500 enfermos e que se diagnostican 19 pacientes novos cada mes. Afecta a duas mulleres por cada varón.
Por outra parte, a EM é a enfermidade neurolóxica non traumática que máis discapacidade causa entre os adultos de entre 20 e 30 anos, cando están iniciando os seus proxectos vitais e o principio da súa vida laboral. Isto dá lugar a unha diminución da produtividade laboral, da capacidade de integración social e da calidade de vida dun grupo de idade especialmente importante dende un punto de vista socioeconómico. Estímase que o custo anual dun paciente con EM é de 26.974 €, o que fai que esta enfermidade se atope entre as 20 que máis custo supoñen para a sociedade.
¿CÓMO SE PRODUCE?
Na actualidade descoñecemos a causa que a produce, se ben o feito de que a súa frecuencia sexa máis do dobre en mulleres que en varóns suxire unha influencia hormonal. Sabemos que non é unha enfermidade infecciosa, que non se contaxia e que non se herda. Os síntomas da enfermidade prodúcense por unha lesión da mielina – sustancia composta por graxas e proteínas que actúa como illante nas fibras nerviosas e que permite a condución normal dos impulsos nerviosos-. Aínda que non coñecemos como se chega a elo, a idea xeral é que o sistema inmunolóxico, que normalmente nos defende das infeccións, ten unha reacción equivocada contra algún dos compoñentes da mielina e dánaa. En función de onde se produza a lesión, aparecerán os diferentes síntomas do doente. O nome da enfermidade débese a que as cicatrices (esclerose) que quedan na zona da lesión poden existir en múltiples zonas do cerebro e/ou da medula espinal.
TIPOS DE EM
Aínda que recentemente se propuxo unha nova clasificación, dende o punto de vista práctico falamos de formas en brotes (remitente-recurrente: RR) e de formas progresivas (secundaria progresiva: SP e primaria progresiva: PP).
Arredor do 85% dos casos son formas RR e nelas o doente sofre episodios de déficit neurolóxico que duran ó menos 24 horas e que se presentan de forma recurrente con repetición de síntomas previos ou con síntomas novos. Estes episodios denomínanse brotes e tras eles pode haber unha recuperación total ou parcial que depende fundamentalmente da capacidade que teña o sistema nervioso de reparar a lesión inflamatoria. Actualmente non é posible predicir cando nin como se vai producir un brote da enfermidade.
Nun 15% de casos o enfermo sofre un deterioro neurolóxico progresivo dende o principio con algúns momentos de empeoramento brusco con recuperación total ou parcial. Son as denominadas formas PP e no seu desenvolvemento predomina o compoñente dexenerativo sobre a inflamación. Nestes casos a proporción home/muller é similar e a idade de aparición é máis tardía, sobre os 40-45 anos.
Entre estas dúas formas da enfermidade está a forma SP, que se presenta na metade dos doentes que padeceron formas RR. Tras moitos anos de padecer brotes, o enfermo ten un empeoramento neurolóxico lentamente progresivo, con ou sen brotes superpostos. Esta forma de evolución intentouse relacionar coa idade de inicio, co número de brotes durante os primeiros 2 anos, co grado de recuperación tras os brotes, cos síntomas ó inicio e co número de lesións en resonancia magnética (RM).
SÍNTOMAS
Van depender da zona do SNC que se afecte, variando entre doentes e dentro dun mesmo enfermo, e poden aparecer como un síntoma neurolóxico único ou como unha combinación de síntomas neurolóxicos.
Trastornos visuais. Son os máis frecuentes e caracterízanse por visión borrosa ou perda de visión con ou sen dor ocular. Soe afectarse un solo ollo. Algúns enfermos refiren visión dobre, xeralmente asociada a outros síntomas neurolóxicos.
Síntomas motores. Son moi variables, dende unha debilidade ou perda total de forza nunha extremidade ou nunha metade do corpo ata unha imposibilidade para a deambulación autónoma. Cando a enfermidade evoluciona pode haber espasticidade, que se describe como rixidez e dificultade para relaxar a musculatura, sobre todo das extremidades inferiores; pode asociarse a espasmos dolorosos que se relacionan con determinadas posturas.
Síntomas sensitivos. Os doentes refiren sensacións variables que van dende cóxegas (parestesias) ata perda de sensibilidade nunha metade do corpo (anestesia). Menos veces poden referir dor ou queimazón nunha extremidade, nunha área determinada do corpo o nunha metade do corpo. En ocasións estes síntomas póñense de manifesto con aumento de temperatura (fenómeno de Uhtoff).
Trastornos de coordinación. Os doentes refiren dificultade para a realización de movementos finos e trastornos da coordinación e/ou equilibrio con marcha inestable. Poden referir visión dobre e dificultade para a deglución de líquidos e para articular palabras.
Trastornos xenitourinarios. Son frecuentes, sobre todo nas formas máis evolucionadas da EM. O máis habitual son episodios de urxencia urinaria con miccións frecuentes e sensación de baleiro incompleto e menos veces hai dificultade para iniciar a micción e/ou retención de ouriños. O estrinximento é máis frecuente que a incontinencia fecal.
Os trastornos da esfera sexual tamén son frecuentes. Ademais da diminución da libido, nos varóns soe caracterizarse por impotencia e trastornos de exaculación e nas mulleres soe ser diminución da sensibilidade e anorgasmia.
Trastornos cognitivos e emocionais. A alteración máis frecuente é a diminución na velocidade de procesamento dos datos e nas formas moi agresivas e con longo tempo de evolución pode haber dende alteración da memoria e da atención ata unha demencia subcortical. Algúns fármacos que se empregan no tratamento sintomático da EM poden influír na súa intensidade o na súa aparición.
O trastorno emocional máis frecuente é a depresión, xeralmente reactiva ó diagnóstico ou á situación funcional que é consecuencia da enfermidade, pero nalgúns casos relacionouse con lesións en determinadas áreas do cerebro. Poucas veces, se hai lesións frontais extensas, pode haber síntomas psiquiátricos e trastornos de conduta.
Síntomas paroxísticos. É a aparición brusca dun síntoma neurolóxico coma dor, inestabilidade, formigueos, trastorno da linguaxe, visión dobre, etc, que dura uns minutos e desaparece. Non teñen relación cun brote e o seu tratamento vai depender da súa intensidade e frecuencia.
Un síntoma moi frecuente da enfermidade é a fatiga. Descríbese como “unha sensación xeneralizada de falta de enerxía” e prodúcese con esforzos mínimos sen que se conseguisen identificar factores desencadeantes coñecidos, aínda que empeora coa calor.
DIAGNÓSTICO
Baséase nunha historia de brotes con signos clínicos nos que se demostra a afectación de máis dun lugar do SNC. Dise que “o doente refire síntomas unilaterais e ten signos bilaterais”. Con eses datos, os estudos complementarios que se teñen que realizar son:
- Análisis do LCR: na EM existen unhas proteínas, as bandas oligoclonais de IgG, que indican actividade inflamatoria no SNC
- Potenciales evocados: los máis empregados son os visuais e é característico un aumento asimétrico da velocidade de condución dos nervios ópticos. Se a lesión é moi intensa pode apreciarse unha alteración da súa morfoloxía
- Resonancia magnética. Aprécianse lesións múltiples no cerebro e/ou na medula espinal que poden brillar tras a administración de contraste. A RM medular pode non realizarse sempre, pero soe ser necesaria nas formas progresivas
Ademais, en todos os doentes realízanse análises de sangue e análises microbiolóxicos e serolóxicos para descartar outros procesos que poden simular unha EM e en casos moi especiais poden precisarse estudos metabólicos e/ou xenéticos máis específicos.
TRATAMENTO
Temos que diferenciar o tratamento do brote, o tratamento sintomático e o tratamento modificador da enfermidade.
1.- Tratamento do brote.
Non sempre é necesario realizalo dado que aínda que pode acortar a súa duración non ten demostrado que mellore o prognóstico a longo prazo. Os brotes trátanse con megadoses intravenosas de metilprednisolona durante 3 ou 5 días, aínda que se pode realizar tratamento por vía oral coas mesmas doses de ese mesmo fármaco. Cando o doente non mellora ou a recuperación é moi parcial poden realizarse entre 3 e 5 sesións de plasmaférese. Non se demostrou que as inmunoglobulinas melloren o resultado dos corticoides.
2.- Tratamiento sintomático.
Buscan a melloría funcional e da calidade de vida do enfermo e non se diferencian dos empregados noutras patoloxías.
- A espasticidade trátase con benzodiacepinas, baclofeno ou tizanidina oral, solos ou combinados e cando se asocia a cambras dolorosas pódense empregar cannabinoides en spray. En casos seleccionados poden ser de utilidade as inxeccións de toxina botulínica.
- O tratamento da dor pode facerse con analxésicos habituais e os episodios paroxísticos soen responder a carbamazepina, gabapentina, pregabalina, fenitoina, amitriptilina ou combinacións destes fármacos.
- No tratamento da urxencia urinaria os máis empregados son a tolterodina, a oxibutinina, a terazosina ou a alfuzosina e cando a resposta é nula ou insuficiente pode asociarse desmopresina ou realizar inxeccións intravesicais de toxina botulínica. O cateterismo vesical intermitente e a cirurxía son outras posibles alternativas.
- A fatiga pode responder a antidepresivos como paroxetina e derivados pero en ocasións responde eficazmente a amantadina, modafinilo ou metilfenidato.
- O trastorno da marcha pode mellorar con fampridina nun 50% dos doentes.
3.- Tratamento modificador da enfermedade.
Consigue diminuír a aparición dos brotes, diminuír a súa intensidade e evitar a progresión da enfermidade e, aínda que a súa eficacia non é absoluta, nos últimos 25 anos demostraron prolongar 10 anos a situación funcional dos doentes cronificando a enfermidade nunha situación funcional mellor que cando non dispoñíamos dos mesmos. Empréganse nas formas RR da EM e algúns deles poden administrarse nas formas SP. Na actualidade non hai tratamento para as formas PP. Estes fármacos teñen indicacións distintas que dependen tanto da agresividade e situación funcional do enfermo como do risco que supón a súa administración e en base a estes parámetros fálase de fármacos de primeira e de segunda liña. Na táboa adxunta recóllense todos os tratamentos dispoñibles na nosa Comunidade.
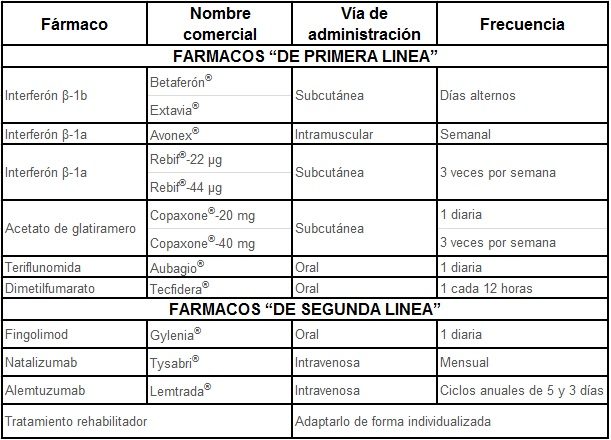
O tratamento rehabilitador debe considerarse coma unha parte imprescindible da atención ó doente dado que a mesma é multidisciplinar e ten que facerse de forma individualizada adaptándoa a cada caso e modificándoa en función da evolución do enfermo. Así, en función de cada doente realizarase fisioterapia, terapia ocupacional, tratamento neuropsicolóxico e/ou logopedia, sen esquecer que a labor da enfermería e da asistencia social tamén forman parte do equipo que debe atender a un doente cun problema neurolóxico crónico.
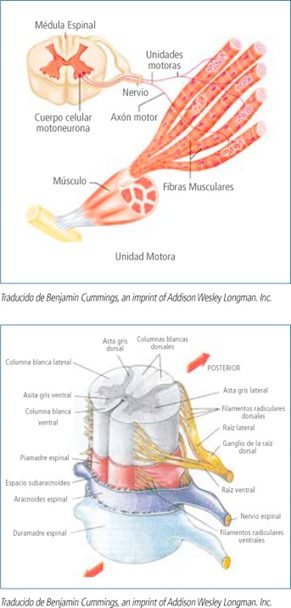
Las enfermedades neuromusculares (ENM) son aquellas que afectan a cualquier componente de la unidad motora (ver imagen), la cual está formada por el músculo, la unión neuromuscular, el nervio periférico y la motoneurona inferior.
Se encuentran dentro del grupo de las denominadas enfermedades raras. En cifras globales, existen más de 50.000 afectados por ENM en toda España.
La mayoría de ellas son enfermedades de origen genético, si bien también pueden ser secundarias a causas adquiridas, como son las enfermedades autoinmunes, inflamatorias o tóxicas.
Dentro de estas enfermedades, la patología más frecuente es la distrofia miotónica, la cual representa un 28% del total.
Las siguientes más frecuentes son las distrofinopatías y la distrofia facio-escápulo-humeral (DFEH), suponiendo un 22.9% y un 10.7% respectivamente.
La atrofia muscular espinal (AME) representa un 5.1%.
Dentro de las neuropatías (las enfermedades que afectan al nervio), entre las más frecuentes se encuentran: la parálisis facial periférica idiopática o de Bell (nervio facial), el síndrome del túnel del carpo (atrapamiento del nervio mediano) o la polineuropatía diabética. Dentro de las hereditarias, la más frecuente es la enfermedad de Charcot-Marie-Tooth.
¿Qué enfermedades se engloban dentro de las enfermedades neuromusculares?
1. ENFERMEDADES DEL MÚSCULO: MIOPATÍAS Y DISTROFIAS MUSCULARES: afectan predominantemente al músculo estriado y son debidas a un defecto en alguna de las proteínas que forman parte de la fibra muscular.
Las miopatías hereditarias y las distrofias musculares son enfermedades de origen genético que pueden iniciarse ya desde la infancia. Provocan una degeneración muscular lenta que da lugar a una debilidad muscular progresiva, con la consecuente discapacidad. Los síntomas principales son la debilidad muscular, la atrofia muscular y las fasciculaciones.
La mayoría de estas enfermedades no tiene un tratamiento efectivo. Es importante mantener actividad física para evitar o mitigar los síntomas motores.
Dentro de este grupo se incluyen las distrofinopatías, las distrofias musculares congénitas y hereditarias, las miopatías hereditarias y congénitas, las enfermedades musculares inflamatorias y las miopatías metabólicas.
2. ENFERMEDADES DE LA UNIÓN NEUROMUSCULAR
2.1 MIASTENIA GRAVIS: Es una enfermedad crónica, autoinmune, de origen desconocido, que se caracteriza por debilidad y fatiga de los músculos esqueléticos (voluntarios) del cuerpo. El problema se encuentra en la unión neuromuscular, encargada de propagar el estímulo eléctrico desde los nervios a los músculos. Esta disfunción se produce por la existencia de unos anticuerpos que destruyen los receptores de acetilcolina bloqueando la transmisión neuromuscular.
Los rasgos característicos de la miastenia son la debilidad muscular fluctuante y la fatiga fácil, que empeoran tras el ejercicio físico y mejoran, total o parcialmente, tras el descanso. La miastenia no produce dolor ni muscular ni articular.
En función de la distribución de los músculos afectados, la MG se clasifica en:
- Ocular: si tras dos años de evolución de la enfermedad la sintomatología solo afecta a los ojos, esto nos puede orientar hacia una forma exclusivamente ocular. Los síntomas típicos son la caída de uno o ambos párpados (ptosis) y la visión nublada o doble.
- Generalizada: si los síntomas aparecen en extremidades (debilidad en las extremidades, alteración de la marcha, dificultad para subir escaleras, dificultad para respirar).
- Bulbar: si afecta a los músculos de la lengua, paladar, masticación y deglución. Da lugar a trastornos del habla (disartria o voz “gangosa”), dificultad respiratoria y dificultad para tragar.
El tratamiento se realiza con diversos fármacos: anticolinesterásicos, inmunosupresores, inmunoglobulinas intravenosas, timectomía y plasmaféresis.
De vital importancia en esta enfermedad es saber que hay determinados fármacos que pueden aumentar la debilidad en algunos pacientes, como son determinados antibióticos (aminoglucósidos, macrólidos, fluoroquinolonas), antihipertensivos y antiarrítmicos y tratamientos hipolipemianes.
2.2- SÍNDROME DE EATON LAMBERT: enfermedad debida a anticuerpos contra componentes de la membrana presináptica de la unión neuromuscular. En un porcentaje elevado de las ocasiones se trata de una enfermedad paraneoplásica, por lo que se debe descartar la presencia de un cáncer oculto.
2.3- SÍNDROMES MIASTÉNICOS CONGÉNITOS: Se trata de enfermedades genéticamente determinadas, que aparecen desde el nacimiento. Se caracterizan por la presencia de fatiga anormal debida a una debilidad muscular localizada o generalizada.
Algunas formas responden de forma parcial a tratamiento con anticolinesterásicos.
Existe una forma adulta de posible comienzo tardío (el síndrome del canal lento).
3. NEUROPATÍAS
Dentro de las neuropatías periféricas, en función del número de nervios afectados y el tipo de afectación, se pueden clasificar en:
- mononeuropatías (solo se afecta un nervio, por ej: síndrome del túnel carpiano)
- polineuropatías (cuando se afectan varios nervios)
- axonales (lesión y degeneración axonal)
- desmielinizantes (lesión de la vaina de mielina)
- neuronopatía (lesión de las neuronas)
La clasificación se basa en el síndrome clínico, los hallazgos patológicos y la etiología. Hay diversas clasificaciones, pero una de las más sencillas y empleadas es dividirlas en agudas y crónicas, simétrica y asimétrica, axonales y/o desmielinizantes.
Existe una amplia variedad de causas que pueden causar daño a los nervios periféricos: carenciales, diabetes, uremia, alcohol, autoinmunes, infecciosas, inflamatorias, fármacos, hereditarias…
Es importante su valoración y diagnóstico precoz, ya que algunos casos son tratables.
4. ENFERMEDADES DE LAS MOTONEURONAS
4.1: MOTONEURONAS INFERIORES: AMIOTROFIAS ESPINALES: grupo de enfermedades caracterizadas por la pérdida o degeneración de las neuronas del asta anterior de la médula espinal. El mal funcionamiento de estas neuronas hace que el impulso nervioso no pueda transmitirse correctamente y, por tanto, los movimientos y el tono muscular se ven afectados. Inicialmente, están mas afectados los músculos proximales y la debilidad en los miembros inferiores suele ser generalmente mayor que la de los miembros superiores. Existen diferentes tipos de Amiotrofias espinales, todas con patrones de herencia autosómico recesivo.
4.2: MOTONEURONAS SUPERIORES E INFERIORES: ESCLEROSIS LATERAL AMIOTRÓFICA: es una de las enfermedades neuromusculares más comunes en el mundo entero y afecta a personas de todas las razas y etnias. La ELA generalmente aflige a personas entre los 40 y 60 años de edad, pero también la pueden desarrollar personas más jóvenes y más viejas. Los hombres son afectados más a menudo que las mujeres. Se trata de una enfermedad neurológica progresiva e invariantemente fatal, que afecta a las neuronas motoras, encargadas de controlar los músculos voluntarios.
Ocasiona debilidad con un rango amplio de discapacidades, afectándose todos los músculos bajo control voluntario. Esto ocasiona pérdida de fuerza y de capacidad para mover el cuerpo y las extremidades. Progresivamente afecta también a la musculatura respiratoria, siendo necesaria la colocación de ventilación artificial si el paciente así lo desea. En la ELA no se afecta la personalidad del paciente, su inteligencia ni su memoria.
Entre el 5 y el 10 por ciento de todos los casos de ELA son heredados. En un 90 a 95 por ciento de todos los casos de ELA, la enfermedad ocurre aparentemente aleatoriamente sin ningún factor de riesgo claramente asociado. Los pacientes no tienen una historia familiar de la enfermedad y no se considera que los miembros de su familia tengan un riesgo mayor de desarrollar ELA.
Hasta la fecha no existe tratamiento curativo. El tratamiento con riluzol ha demostrado un aumento de la supervivencia de varios meses, sobre todo en aquellos pacientes con dificultad para tragar y prolonga el tiempo antes que el paciente necesite soporte ventilatorio. Otros tratamientos están destinados a mejorar la calidad de vida del paciente y a aliviar los síntomas, como son los antidepresivos, laxantes, analgésicos, terapia física, logopedia…
¿Qué síntomas orientan a la existencia de una enfermedad neuromuscular?
- Trastorno de la marcha: las características de la marcha típica de un paciente con enfermedad neuromuscular son el bamboleo, la fatigabilidad, la asimetría, la claudicación y la marcha en punta de pies. Esta marcha es típica de las miopatías y distrofias musculares, aunque también se puede ver en las miastenias y en las atrofias musculares espinales. La fatigabilidad puede indicar un síndrome miasteniforme o a una miopatía mitocondrial.
- Caídas frecuentes: se producen principalmente por debilidad muscular proximal (más cerca al tronco) o distal (más lejos del tronco) de las extremidades inferiores.
- Dificultades para subir y/o bajar escaleras.
- Dolor muscular relacionado o no con el ejercicio.
- Dificultad para ponerse en pie desde el suelo. Este síntoma se conoce como Signo de Gowers. Los pacientes no son capaces de levantarse desde el suelo sin apoyar una o las dos manos en el suelo. Para compensarlo, los pacientes suben apoyándose en sus propias piernas.
- Calambres: son espasmos o contracturas dolorosas. Se observan sobre todo en las enfermedades que afectan al músculo.
- Dificultades de alimentación, atragantamientos. Sobre todo en aquellas entidades que cursan con debilidad de la musculatura bulbar, que permite tragar. Durante meses puede ser la única manifestación del a miastenia gravis.
- Infecciones respiratorias frecuentes y/o prolongadas. Se producen por dificultad para toser y mantener la vía respiratoria limpia. Puede llegar a existir una insuficiencia respiratoria restrictiva.
- Trastornos del sueño: en ocasiones las alteraciones respiratorias pueden manifestarse inicialmente solo durante le sueño, dando lugar a la aparición de despertares nocturnos frecuentes, sensación de ahogo, ortopnea (dificultad respiratoria al estar tumbado), cefalea matinal y cansancio durante el día. Estos síntomas pueden estar indicando una retención de CO2. La entidad que mayor tasa de trastornos de sueño produce es la distrofia miotónica, apareciendo hasta en el 80% de los pacientes.
- Visión doble: por afectación de la musculatura extraocular. Se observa sobre todo en la miastenia gravis, el síndrome de Miller Fisher y en enfermedades mitocondriales.
En la exploración física podemos encontrar:
- Debilidad muscular
- Atrofia muscular, llamada amiotrofia.
- Talla baja o bajo peso
- Cambios en la piel
- Contracturas articulares progresivas
- Escoliosis progresiva
- Hipertrofia muscular. Al contrario de la atrofia muscular, la hipertrofia es un aumento de tamaño de la musculatura esquelética. La musculatura más habitualmente hipertrofiada es la de las pantorrillas, la cual se observa sobre todo en distrofinopatías, al igual que la hipertrofia lingual.
- Contracciones musculares involuntarias: rippling, fasciculaciones y miotonía.
- Hiperlaxitud distal.
- Deformaciones torácicas: pectum carinatum/pectum excavatum. Se produce por compromiso y debilidad de la musculatura torácica.
- Ausencia de reflejos osteotendinosos: en la mayoría de enfermedades neuromusculares, si bien hay entidades que cursan con reflejos vivos, como son determinadas atrofias espinales y enfermedades de motoneuronas.
- Pie cavo: signo clásico de la neuropatía de Charcot-Marie-Tooth.
- Luxaciones de la rótula.
- Temblor fino de manos y temblor de lengua. Por pérdida de neuronas motoras.
- Ptosis palpebral (párpado caído) y oftalmoplejia. Aparecen típicamente en las miastenias, en las miopatías mitocondriales y en algunas miopatías congénitas.
- Paladar ojiva.
- Voz nasal
¿Qué otros órganos se pueden afectar en algunas enfermedades neuromusculares?
El compromiso de otros órganos o tejidos es común en varias de las ENM. Los más importantes a tener en consideración son el compromiso cardíaco, donde se pueden encontrar miocardiopatías dilatadas, restrictivas o alteraciones del ritmo cardíaco con arritmias y fibrilaciones ventriculares, entre otras. Pueden ser causa de muerte súbita y necesitar la implantación de marcapasos o desfibriladores de forma preventiva para evitar muerte súbita.
También se puede afectar la función hepática, con aumento de transaminasas. Suele aparecer en las enfermedades que afectan al músculo, como las glucogenosis y también a las enfermedades mitocondriales.
En determinadas enfermedades pueden existir alteraciones endocrinológicas, como intolerancia a la glucosa, resistencia a la insulina y diabetes mellitus. En algunas miopatías mitocondriales puede existir hipotiroidismo e hipoparatiroidismo.
En algunas distrofias musculares puede existir compromiso cognitivo en grado variable.
Es frecuente también el compromiso ocular y auditivo, que ocurren en pacientes con distrofias musculares, miopatías mitocontdriales.
La constipación crónica frecuente es una manifestación del compromiso gastrointestinal que se produce por
¿Cómo se realiza el diagnóstico de una enfermedad neuromuscular?
Además de la historia clínica y de la exploración física y neurológica, suele ser necesaria la realización de pruebas complementarias para poder llegar a un diagnóstico certero.
Estas pruebas complementarias suelen ser:
- Analítica general con estudio de hormonas tiroideas y enzimas musculares, autoinmunidad, etc.
- Electroneuromiograma: en donde se estudia el funcionamiento de los nervios periféricos, el músculo y la unión entre los dos.
- Punción lumbar: mediante la cual se toman muestras de líquido cefalorraquídeo, cuyo análisis es imprescindible para el diagnóstico de determinadas enfermedades.
- Pruebas de imagen: resonancia magnética, tomografía computerizada (TC). Principalmente se realizan para descartar otras enfermedades que puedan simular una enfermedad neuromuscular o bien para estudio del músculo.
- Biopsia muscular: puede ser necesaria para precisar el tipo de miopatía. Existen cambios musculares característicos en determinadas enfermedades como son las miopatías inflamatorias, la miositis por cuerpos de inclusión, distrofias musculares…
- Estudio genético: cada vez su uso está en aumento permitiendo confirmar y categorizar determinadas enfermedades neuromusculares, en la mayoría de los casos hereditarias.


 Español
Español